No dinâmico cenário do tratamento da infecção pelo HIV, precisamos sempre rediscutir e repensar nossas estratégias à luz das novas evidências científicas e das diferentes situações epidemiológicas. Assim, o estímulo expresso nos diferentes protocolos e diretrizes – incluindo os Protocolos Clínicos e Diretrizes Terapêuticas (PCDT) do Ministério da Saúde do Brasil – quanto ao tratamento precoce e universal de todos os pacientes que vivem com HIV tem levado a uma exposição cada vez maior desses pacientes aos esquemas de primeira linha, o que traz grandes desafios às unidades de saúde em relação ao acolhimento, à retenção no cuidado e ao estímulo à adesão. Considerando-se a reduzida barreira genética do esquema proposto para tratamento inicial em áreas de recursos limitados, composto geralmente por efavirenz (EFV) associado ao tenofovir (TDF) + lamivudina (3TC), e o aumento progressivo nas taxas de resistência transmitida com impacto principalmente na classe dos inibidores de transcriptase reversa não análogos de nucleosídio (ITRNN), 1 é possível prever que teremos cada vez mais pacientes em falha terapêutica, para os quais será necessário pensar em esquemas de resgate.
Identificando a falha virológica
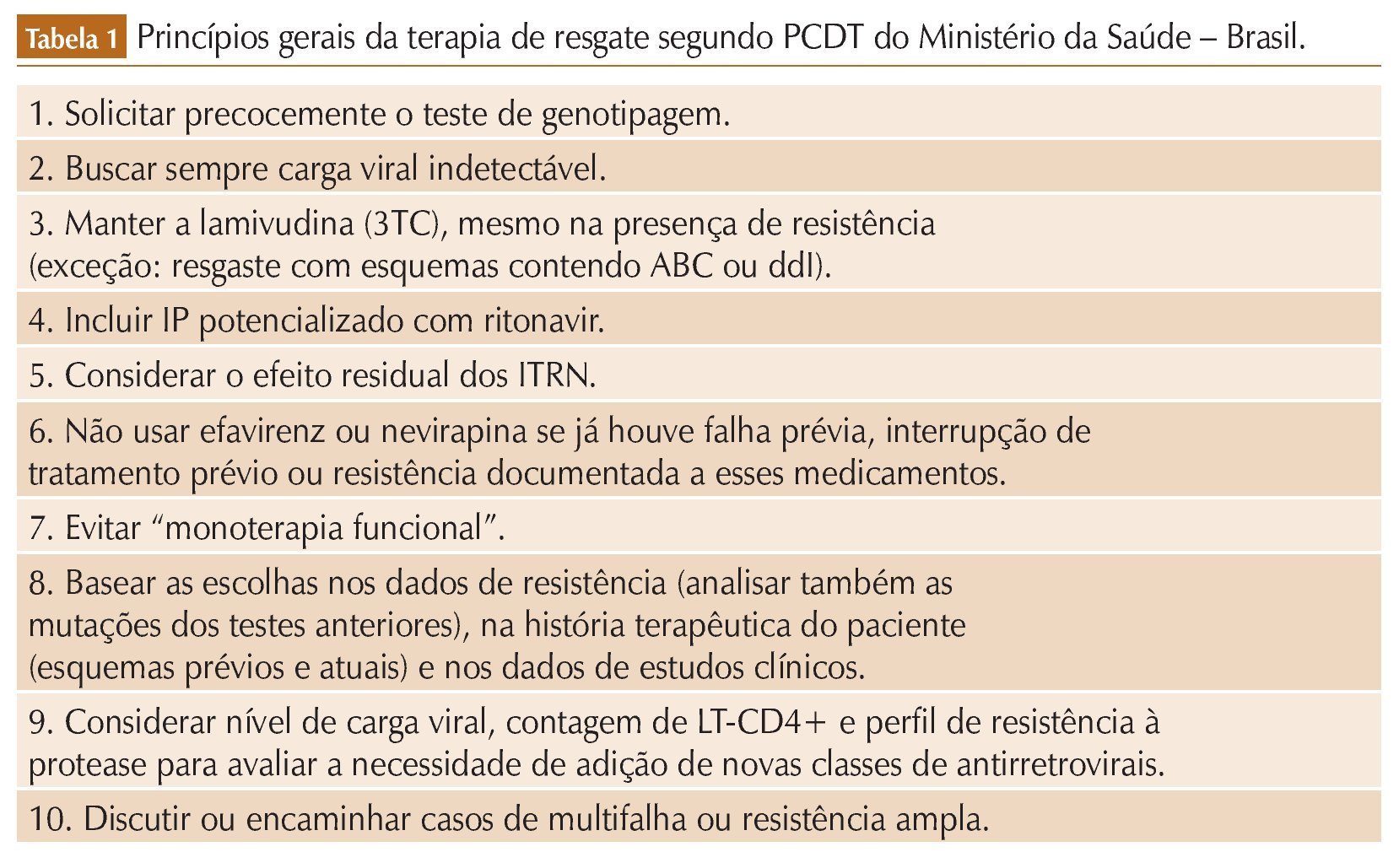
A seção do nosso PCDT dedicada ao resgate traz indicações gerais sobre os pontos que devem nortear esse processo2 (tabela 1). Como princípio, os especialistas recomendam a identificação precoce da falha terapêutica. Esse é, ainda hoje, um dos elementos mais importantes para limitar as consequências deletérias da falha – não somente o risco de progressão da doença associado à replicação viral, mas também a perda de opções terapêuticas pela seleção adicional de mutações associadas à resistência viral relacionada à pressão seletiva da manutenção de um esquema antirretroviral ineficaz.
Assim, a conduta frente aos pacientes sem supressão viral adequada é a confirmação quanto à presença de carga viral (CV) detectável após quatro semanas do primeiro exame. Em seguida, deve-se tentar obter um teste de resistência pelo exame de genotipagem. Embora, de uma forma geral, esse teste só deva ser solicitado após seis meses de terapia antirretroviral regular (casos em que a resposta virológica pareça claramente inadequada, como a queda < 1 log após um mês ou < 2 logs nos primeiros três meses de tratamento), também deve ser seguido de perto, principalmente em esquemas baseados em ITRNN, podendo refletir, nessas situações, a presença de resistência transmitida.
Um caso particularmente difícil é o paciente que mantém viremia reduzida, entre 50-200 cópias/mL, uma vez que nesses níveis o teste de resistência é de difícil realização. De uma forma geral, a viremia em níveis reduzidos está associada a um risco menor de seleção de cepas resistentes, mas há evidências de que isto pode ocorrer mesmo nesse contexto.4 Deve-se monitorar de perto e, havendo sinais de que não seja possível manter a supressão viral, avaliar a introdução de um esquema de resgate.
De uma forma geral, a viremia em níveis reduzidos está associada a um risco menor de seleção de cepas resistentes, mas há evidências de que isto pode ocorrer mesmo nesse contexto.
Efeito dos inibidores de transcriptase reversa análogos de nucleosídio no resgate
Dados de estudos recentes lançaram luz aos nossos conhecimentos sobre esquemas de segunda linha. Dois estudos de desenho semelhante compararam a eficácia de 2-3 inibidores de transcriptase reversa análogos de nucleosídio (ITRN) combinados com lopinavir/ritonavir (LPV/r) com terapia dupla formada por raltegravir (RAL) e LPV/r, após falha ao esquema inicial composto por ITRNN + 2 ITRN.5,6 Os resultados finais de ambos foram semelhantes em relação à taxa de supressão viral < 50 cópias/mL na semana 48. Um terceiro braço em que a terapia dupla LPV/r + RAL era mantida apenas por três meses e depois trocada para LPV/r em monoterapia apresentou indícios de falha virológica bem mais elevada.
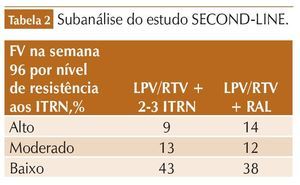
O dado mais surpreendente veio de uma análise de um desses estudos, que demonstrou que a taxa de eficácia do braço com ITRN + LPV/r era maior quando a genotipagem realizada antes do tratamento (não disponível no momento da randomização) mostrava níveis de resistência mais elevados7 (tabela 2). Esse falso paradoxo, na verdade, reflete o fato de que a presença de níveis mais baixos de resistência aos ITRN no momento da falha provavelmente marca um grupo de pior adesão, uma vez que o uso correto de drogas dessa classe selecionaria mutações de resistência. Esses resultados mostram, mais do que nunca, o efeito residual significativo dos ITRN mesmo na presença de resistência viral documentada para essa classe.
Os casos em que são encontradas mutações de resistência na protease com impacto significativo na atividade dessa classe tendem a ser bem mais complexos.
A escolha do inibidor de protease reforçado com ritonavir
A escolha específica do inibidor de protease reforçado com ritonavir (IP/r) também é um fator importante a ser considerado na construção de um esquema de resgate. Embora o LPV/r ainda seja considerado o IP/r de escolha no Brasil, diversos estudos sugerem que possa haver pior tolerabilidade desse IP quando comparado a outros medicamentos da mesma classe, como o atazanavir/r (ATV).8 A eficácia, no entanto, na ausência de mutações de resistência na protease, é semelhante, devendo ser consideradas as características de cada droga dentro da classe. O ATV/r, assim como o fosamprenavir/r (F-APV/r)m – este último apenas na ausência de mutações primárias na protease – poderiam ser beneficiados pela dose única diária e melhor tolerância gastrintestinal. O LPV/r tem como característica mais importante a coformulação, o que impede seu uso sem o efeito booster do ritonavir, limitando a possibilidade de seleção de resistência na protease mesmo no contexto de uma adesão inadequada.9
Esquemas de terceira linha
Os casos em que são encontradas mutações de resistência na protease com impacto significativo na atividade dessa classe tendem a ser bem mais complexos. Torna-se essencial discutir, nessas situações, além da escolha adequada do melhor IP/r, também o número de drogas ativas necessárias.
O desenvolvimento de uma nova geração de IP/r chamada de não peptídicos, o tipranavir/r (TPV/r) e o darunavir/r (DRV/r), demonstrou que essas drogas eram mais eficazes que IP/r comparadores escolhidos por meio do teste de resistência.10,11 Mais especificamente, no caso do DRV/r foi observada uma atividade superior em comparação com o LPV/r, mesmo em situações nas quais, a despeito da presença de mutações de resistência na protease, havia ainda sensibilidade fenotípica a ambas as drogas.12 Esses dados sugerem que o DRV/r deve ser o IP escolhido para compor o esquema antirretroviral em todas as situações em que haja mutações com impacto a múltiplos agentes dessa classe, como substituições nas posições 46, 54, 82 e 90. O TPV/r, por apresentar problemas específicos de tolerabilidade e segurança associados à dose elevada de ritonavir necessária (400 mg/dia), além de aspectos de interações farmacológicas com drogas potencialmente úteis no resgate, ficaria restrito a situações específicas nas quais ele resta como único agente com atividade demonstrável.
O MRV tem a seu favor o fato de representar uma classe nova, os antagonistas de CCR5, uma citocina que funciona como um correceptor necessário para a entrada do vírus nas células CD4.
Número de drogas ativas
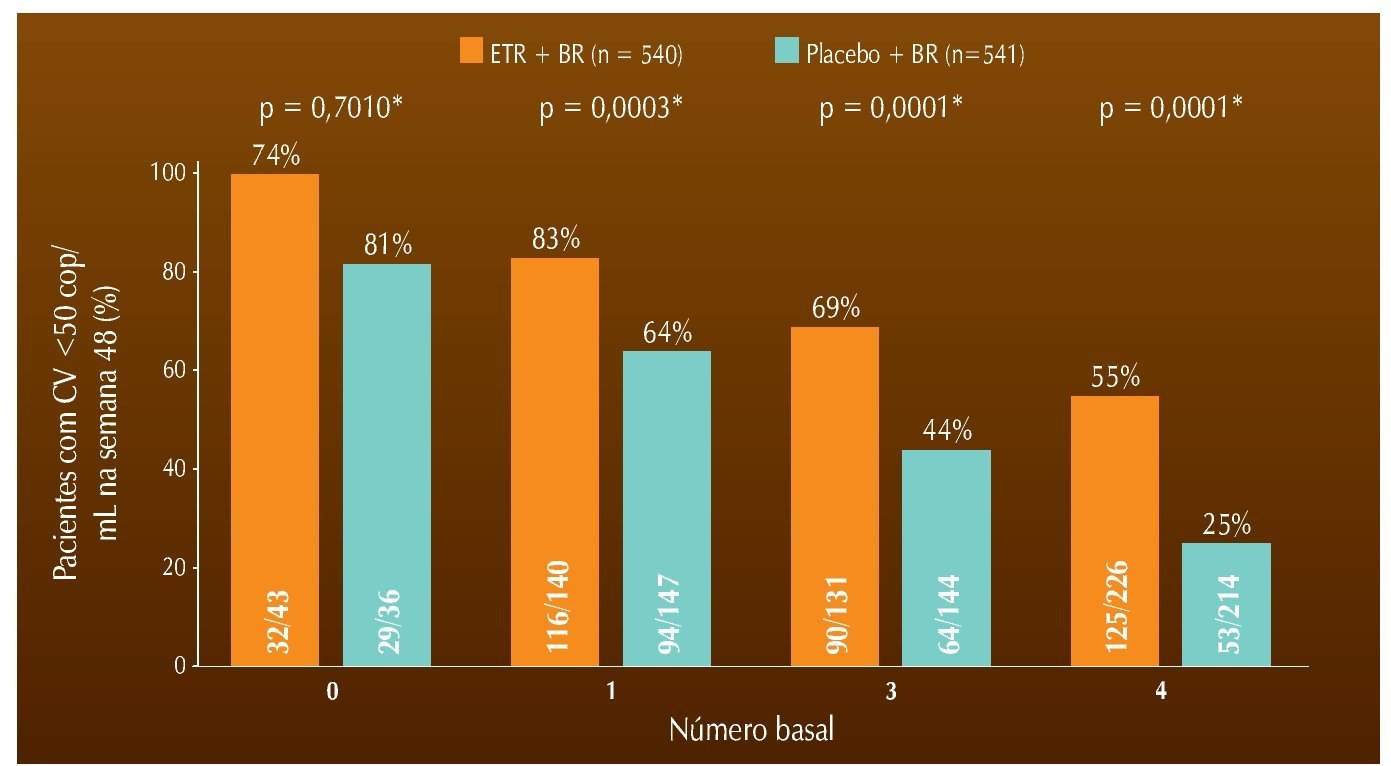
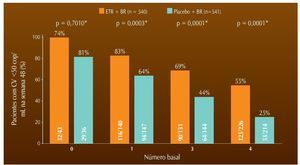
Pelos resultados dos estudos SECOND-LINE e EARNEST, está claro, que na presença de um IP/r sem a ocorrência de mutações primárias de resistência na protease, os ITRN devem contar como droga ativa. Nesse contexto, alguns resultados significativos podem ser encontrados nos estudos DUET, usados na etapa de registro da etravirina (ETR), nos quais a terapia de base de todos os pacientes continha DRV/r.13 Na ausência de mutações do grupo de 11 que comprometam a atividade desse IP, a ETR não foi superior ao placebo quando combinada ao DRV/r + base de ITRN.14 Na presença de uma mutação, no entanto, essa diferença já era demonstrável; com mais de uma mutação, a atividade parece ser reduzida, mesmo na presença da ETR, sugerindo a necessidade de mais uma droga ativa (fig. 1).
Figura 1 Resposta à etravirina segundo número de mutações para darunavir/ritonavir.
Deve ser lembrado também que, na ordem de entrada de novas classes determinada pelas diretrizes do PCDT brasileiro em pacientes com histórico de falha, dentre as três classes mais frequentemente empregadas em nosso país (ITRN, ITRNN, IP), o RAL deve ser a primeira droga a ser utilizada, por representar uma nova classe à qual o paciente ainda não foi exposto (ao contrário da ETR) e cuja atividade pode ser inferida sem a necessidade de testes específicos (como é o caso do maraviroque – MRV). Nesse caso, é importante que o esquema tenha atividade confiável, pois a falha com uso de RAL leva, frequentemente, à seleção de cepas resistentes a essa classe com potencial de comprometer, inclusive, outras alterativas entre os inibidores de integrase (INI). Deve-se evitar, por exemplo, o resgate com terapia dupla RAL/r + IP/r, mesmo na ausência de mutações de resistência a esse último, uma vez que o risco de falha nessa situação é tão grande quanto o uso de IP/r com ITRN reciclados, e a consequência da falha muito mais danosa, pelo risco de resistência aos INI. Nessa situação, deve-se manter a base de ITRN ou acrescentar uma nova classe, pelo menos até a supressão viral adequada.
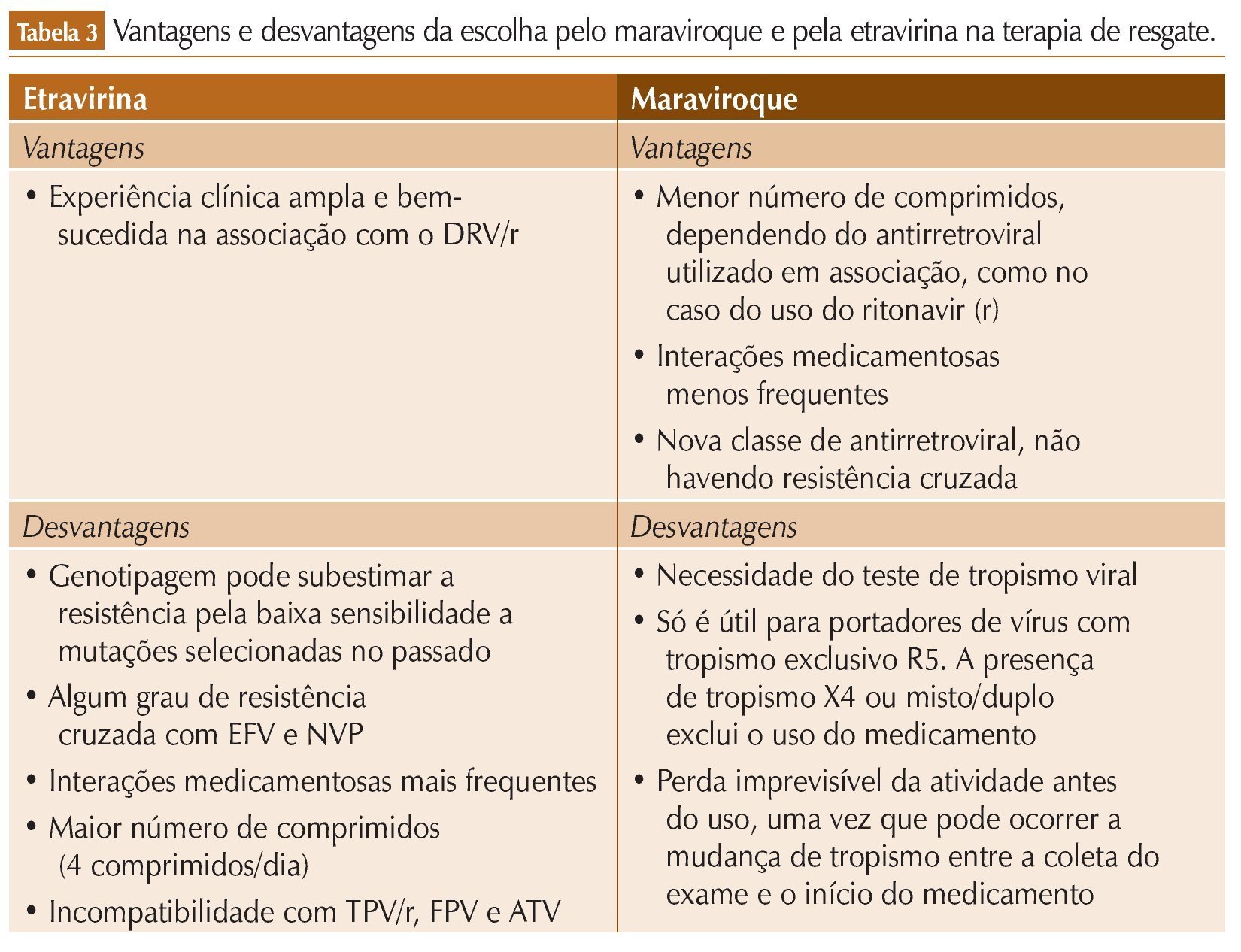
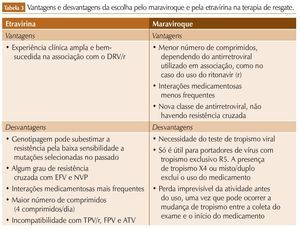
A partir dos INI, a ordem de entrada é menos definida. As duas opções para via oral – MRV e ETV – têm seus prós e contras ressaltados nas diretrizes do Ministério da Saúde brasileiro (tabela 3). O MRV tem a seu favor o fato de representar uma classe nova, os antagonistas de CCR5, uma citocina que funciona como um correceptor necessário para a entrada do vírus nas células CD4. Apresenta também um perfil de segurança satisfatório, pois não foram identificados eventos adversos significativos após cinco anos de observação em estudos controlados.15 Sua atividade, no entanto, precisa ser documentada por meio de um teste de tropismo, já que na evolução natural da infecção pelo HIV encontramos uma mudança a partir da qual o vírus passa a utilizar outra citocina como correceptor, a CCXR4, o que anula a atividade antiviral dos agentes dessa classe. Isso coloca a decisão sobre a sua utilização numa encruzilhada; por um lado, há uma tendência a querer usála precocemente, uma vez que é uma droga que pode ser perdida mesmo sem a sua utilização. Por outro, há um receio de que a mudança de tropismo possa ocorrer mesmo entre a realização do teste e o início do medicamento, fato que já foi demonstrado em estudos clínicos. O risco de que isso aconteça e o tempo de validade desse teste são difíceis de definir; dados do estudo MOTIVATE, no entanto, parecem fornecer uma pista. No período entre a inclusão no estudo, quando todos os pacientes deveriam ter um teste mostrando tropismo para CCR5, e o início do tratamento, com um intervalo de até seis semanas, foi possível observar uma mudança de tropismo em cerca de 8% dos voluntários,16 o que seria um indício do risco de que esse evento possa ocorrer nesse mesmo prazo se a medicação demorar a ser iniciada. Entretanto, os autores colocam como provável causa desta mudança a baixa sensibilidade do teste de tropismo utilizado, para detecção de variantes X4.
A ETR, por sua vez, tem a seu favor uma ampla experiência clínica com o DRV/r, IP/r de escolha em esquemas de terceira linha e que não foi utilizado no estudo MOTIVATE. Há também o reforço dos dados do estudo TRIO, de braço único, que utilizou DRV/r + RAL + ETR em 103 pacientes com mutações principais de resistência para IP e ITRNN, encontrando uma eficácia de 86% até a semana 48, comparável à de esquemas de primeira linha.17 Por outro lado, não se trata de um medicamento de classe nova e pode ter sua atividade comprometida por mutações selecionadas previamente após falha a esquemas contendo ITRNN, geralmente utilizados como primeira linha, que podem não ser identificados em um momento posterior quando o uso da droga estiver sendo considerado.
O fato mais importante relacionado à terapia de resgate nos últimos anos foi o aparecimento de um novo INI, o dolutegravir (DTG).
Tendências atuais e perspectivas
Sem dúvida, o fato mais importante relacionado à terapia de resgate nos últimos anos foi o aparecimento de um novo INI, o dolutegravir (DTG). Essa medicação parece manter a potência intrínseca e o excelente perfil de segurança comuns à classe, agregando, no entanto, uma característica até então ausente: a barreira genética. De fato, em nenhum dos estudos clínicos realizados no processo de desenvolvimento da medicação em pacientes virgens de tratamento, envolvendo ao todo aproximadamente 1.000 pacientes em uso de DTG combinado com base de ITRN (TDFr/emtricitabina ou abacavir (ABC)/3TC), foram identificadas mutações de resistência no momento da falha virológica.18-20 Esse perfil é comparável ao da classe dos IP/r e sugere a perspectiva de um novo gargalo para prevenção do surgimento de vírus multirresistente.
A análise do estudo clínico SAILING, no qual o DTG e o RAL foram comparados lado a lado para uso em esquemas de resgate em pacientes sem história de uso prévio de INI, mostrou aspectos ainda mais interessantes. Na semana 48, 71% dos pacientes no braço DTG e 64% dos pacientes no braço RAL apresentavam RNA do HIV < 50 cópias/mL. A diferença a favor do DTG de 7,4%, com intervalo de confiança de 95% de 0,7 a 14,2, foi considerada estatisticamente significativa.21
As análises post hoc também trouxeram importantes contribuições sobre os efeitos específicos em determinados subgrupos. Avaliando especificamente os pacientes que fizeram DRV-r em seus esquemas de base otimizados, mas que apresentavam mutações primárias na protease, a diferença na eficácia até a semana 48 ficou ainda mais evidente: 85% dos pacientes versus 67% no braço RAL. Esse resultado reforça o papel específico do DTG de resgatar a barreira genética do esquema, perdida após a seleção de mutações na protease, para que seja garantida a durabilidade da sua eficácia.
Outro resultado digno de nota é relacionado à análise dos pacientes que utilizaram apenas ITRN em seus esquemas de base. Foram 32 pacientes em cada grupo. Em nenhum dos pacientes no braço DTG houve falha virológica, contra sete pacientes que apresentaram esse desfecho no braço RAL. Se observarmos que em apenas metade desses pacientes ambos os ITRN se encontravam plenamente ativos pelos testes de resistência realizados, podese prever uma interessante perspectiva para o uso de DTG em esquemas de segunda linha sem a necessidade de IP/r. De fato, essa estratégia já é alvo de estudo clínico em andamento.
No estudo SAILING foi possível colocar à prova também a barreira genética do DTG, uma vez que pela primeira vez a droga era usada em pacientes ainda sem experiência com a classe dos INI, porém com esquemas de base nem sempre de atividade confiável. Ao todo, foram registrados quatro pacientes com mutações de resistência na integrase, contra 17 no braço RAL, diferença estatisticamente significativa (p = 0,003). Em um desses quatro foi demonstrada a presença de mutações na integrase já na entrada no estudo (148H-140S), sugerindo uso prévio da classe. Dois outros apresentavam uma substituição identificada anteriormente em estudos in vitro – a 263K –, que confere apenas uma discreta redução de aproximadamente duas vezes na suscetibilidade à droga, sem impacto significativo na resistência fenotípica. O outro paciente apresentou CV elevada em todas as visitas de seguimento, e foi identificado um polimorfismo no momento da constatação da falha virológica na posição 151, que não compromete a atividade de nenhum dos medicamentos conhecidos dessa classe.
A incorporação do DTG representa, portanto, uma importante contribuição ao nosso arsenal terapêutico. É possível, com seu uso, compor esquemas de resgate de durabilidade confiável mesmo quando o DRV/r já estiver com sua atividade potencialmente comprometida pela presença de mutações de resistência na protease. Será possível, até mesmo, poupar outras drogas de novas classes nessa circunstância, algo que não deve ser feito com o RAL.
Dada a importância dos INI, é preciso que o uso de agentes dessa classe com maior vulnerabilidade às mutações de resistência, como é o caso do RAL, seja feito de maneira consciente, evitando-se a exposição dessa droga em esquemas de atividade subótima (menos de duas drogas ativas, especialmente se a única droga ativa não for um IP/r sem mutações de resistência) e identificando precocemente a falha virológica a fim de preservar opções terapêuticas. Já foi possível demonstrar que o perfil mutacional associado ao momento inicial da falha virológica contendo RAL é caracterizado pela substituição da posição 155, que em geral não demonstra impacto significativo na atividade do DTG. A persistência da falha, no entanto, em um espaço de tempo relativamente curto de oito a doze semanas, leva a uma mudança nesse perfil, passando a predominar o grupo de substituições nas posições 148-140,22 que reduzem a atividade do DTG e colocam em risco a seleção de mutações adicionais, mesmo com o uso dessa droga em dose dobrada.
Situações especiais
Um dos pontos relacionados ao resgate é a importância de se buscar sempre a CV indetectável, uma vez que somente assim é possível obter benefícios clínicos duradouros e evitar a progressão para multirresistência. No entanto, a fatores relacionados à limitação de opções terapêuticas, podem impor dificuldades a essa meta, especialmente em áreas onde há restrições a novos agentes como o DTG. O encaminhamento para centros de referência pode ser importante nesse momento, principalmente àqueles com atividade de pesquisa em novas opções terapêuticas.
Conclusões
O desenvolvimento de novos agentes para terapia antirretroviral nos últimos 10 anos nos permite, atualmente, estender os benefícios do tratamento à maioria dos pacientes que vivem com HIV, mesmo aqueles com histórico de falha a diversos esquemas anteriores. É possível, ainda, identificar dois agentes, o DRV/r e o DTG, considerados como preferenciais para início de tratamento em diversas diretrizes,23 que até o momento não estão associados à seleção de cepas resistentes em esquemas de primeira linha, criando a partir da primeira exposição ao tratamento uma barreira expressiva contra esse risco.
Podemos observar, no entanto, que o ritmo de desenvolvimento de novos agentes tem se alentecido no período mais recente. Isso aumenta ainda mais a nossa responsabilidade em usar de maneira adequada os nossos recursos, valendo-se de todas as evidências disponíveis, procurando também, sempre que possível, investir de modo consciente para ampliar esses recursos, incorporando estratégias que possam representar claramente um avanço no cuidado das pessoas que vivem com HIV.